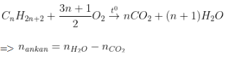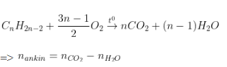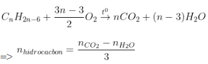Lý thuyết hoá hữu cơ rất nhiều vì vậy phần bài tập cũng rất đa dạng. Để các em làm tốt các dạng bài tập phần hóa hữu cơ, Kiến Guru cung cấp cho các em Các công thức hoá học lớp 11 để giúp giải nhanh bài toán hiđrocabon.
I. Các công thức hoá học lớp 11: Toán đốt cháy Hidrocacbon
- Công thức tổng quát của một hiđrocabon (HC): CxHy (x, y nguyên dương) hoặc
CnH2n + 2 -2k với k là số liên kết π và vòng trong hiđrocabon.
- Công thức tính số π + v: π + v = 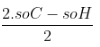
- Phương trình đốt cháy: 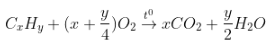
- Dựa vào số mol CO2 và H2O sau phản ứng ta có thể xác định được loại hợp chất.
|
Quan hệ mol CO2 và H2O |
Loại hiđrocabon |
Phương trình |
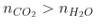 |
Ankan |
|
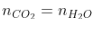 |
Anken |
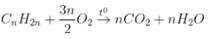 |
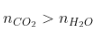 |
Ankin, Ankađien |
|
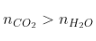 |
Đồng đẳng benzen |
|
- Các định luật bảo toàn thường sử dụng:
+ Bảo toàn khối lượng: 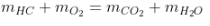
+ Bảo toàn nguyên tố:
|
Bảo toàn C: |
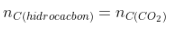 |
|
Bảo toàn H: |
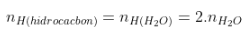 |
|
Bảo toàn O: |
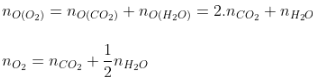 |
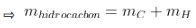 (trong thành phần phân tử chỉ chứ C và H).
(trong thành phần phân tử chỉ chứ C và H).
- Công thức tính số C, số H:
+ Số C = 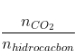
+ Số H = 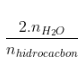
- Đối với các bài toán đốt cháy hỗn hợp 2 hiđrocabon thì:
+ Khối lượng mol trung bình: 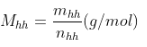
hoặc 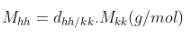 hoặc
hoặc 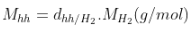
+ Số Ctb = 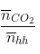
Lưu ý: Khi số C trung bình là số nguyên (bằng trung bình cộng của 2 số nguyên tử C) thì số mol 2 chất bằng nhau.
- Bài toán sử dụng hỗn hợp sản phẩm để tiếp tục cho tham gia phản ứng:
+ Dẫn sản phẩm cháy qua bình (1) đựng P2O5, H2SO4 đặc, CaO, muối khan,.... rồi dẫn qua bình 2 đựng dung dịch bazơ như NaOH, Ca(OH)2,...
mbình 1 tăng = mH2O (hấp thụ nước)
mbình 2 tăng = mCO2 (hấp thụ CO2).
+ Dẫn toàn bộ sản phẩm cháy đi qua bình đựng dung dịch bazơ như NaOH, Ca(OH)2,...
mbình tăng = mCO2 + mH20 (hấp thụ cả CO2 và nước).
+ Khối lượng dung dịch tăng: m dd tăng = mCO2 + mH20 – m kết tủa .
+ Khối lượng dung dịch giảm: m dd giảm = m kết tủa – (mCO2 + mH20 ).
+ Lọc bỏ kết tủa, đung nóng dung dịch lại thu được kết tủa nữa:
PT: 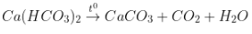
Các công thức hoá học lớp 11
II. Các công thức hoá học lớp 11: Tính số đồng phân Hidrocacbon
1. Đồng phân ankan:
- CTTQ: CnH2n+2 (n ≥ 1)
- Ankan chỉ có đồng phân mạch cacbon và từ C4 trở đi mới có đồng phân.
- Công thức tính nhanh: 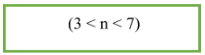
2. Đồng phân anken:
- CTTQ: CnH2n (n ≥ 2).
- Anken có đồng phân mạch C, đồng phân vị trí nối đôi và đồng phân hình học.
- Mẹo tính nhanh đồng phân anken:
Xét 2C mang nối đôi, mỗi C sẽ liên kết với 2 nhóm thế (giống hoặc khác nhau).
Ví dụ với C4H8: Trừ đi 2C mang nối đôi sẽ còn 2C và H nhóm thế.
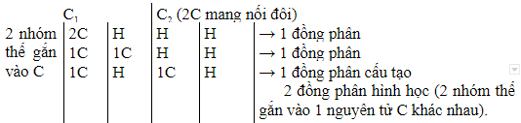
Nếu đề bài yêu cầu tính đồng phân cấu tạo sẽ là: 1+1+1=3 đồng phân. Nếu yêu cầu tính đồng phân (bao gồm đồng phân hình học) sẽ là 1+1+2=4 đồng phân.
3. Đồng phân ankin:
- CTTQ: CnH2n-2 (n ≥ 2).
- Ankin có đồng phân mạch C, đồng phân vị trí nối ba và không có đồng phân hình học.
- Mẹo tính nhanh đồng phân ankin:
Xét 2C mang nối ba, mỗi C sẽ liên kết với 1 nhóm thế (giống hoặc khác nhau).
Ví dụ với C4H6: Trừ đi 2C mang nối ba sẽ còn 2C và H là nhóm thế.
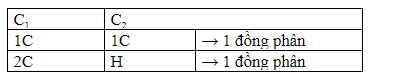
Ta có 2 đồng phân ankin.
4. Đồng phân benzen:
- CTTQ: CnH2n-6 (n ≥ 6).
- Công thức tính số đồng phân: 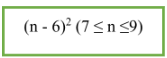
5. Đồng phân ancol:
- CTTQ của ancol no, đơn chức, mạch hở: CnH2n+1OH hay CnH2n+2O (n ≥ 1).
- Ancol có đồng phân mạch C và đồng phân vị trí nhóm OH.
- Công thức tính số đồng phân: 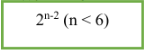
6. Đồng phân ete:
- CTTQ của ete no, đơn chức, mạch hở: CnH2n+2O (n ≥ 2).
- Công thức tính số đồng phân: 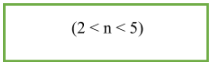
7. Đồng phân phenol:
- CTTQ: CnH2n-6O (n ≥ 6)
- Công thức tính nhanh: 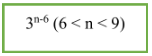
8. Đồng phân anđehit:
- CTTQ của anđehit no, đơn chức, mạch hở: CnH2nO (n ≥ 1). Trong phân tử chứa một nối đôi ở nhóm chức CHO.
- Công thức tính nhanh: 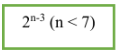
9. Đồng phân xeton:
- CTTQ của xeton no, đơn chức, mạch hở: CnH2nO (n ≥ 3). Trong phân tử chứ một nối đôi ở nhóm chức CO.
- Công thức tính số đồng phân: 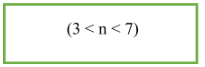
10. Đồng phân axit:
- CTTQ của axit no, đơn chức, mạch hở: CnH2nO2 (n ≥ 1). Trong phân tử chứa một nối đôi ở nhóm chức COOH.
- Công thức tính số đồng phân: 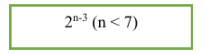
III. Các công thức hoá học lớp 11: Phản ứng thế Halogen
- Đây là phản ứng đặc trưng của ankan.
1. Dẫn xuất monohalogen:
- Ankan + Halogen tỉ lệ 1 : 1 thu được dẫn xuất monohalogen.
- Yêu cầu của đề: xác định công thức ankan
- PT: 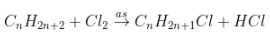
hoặc 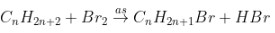
- Dữ kiện: đề bài sẽ cho %C, %H, hay %Halogen.
- Công thức tính:
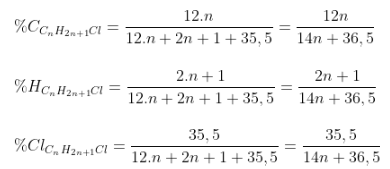
Kết hợp với dữ kiện đề cho, tìm n.
- Sau khi xác định được CTPT, dựa vào số lượng sản phẩm thế để tìm CTCT của ankan. Khi phản ứng với halogen cho sản phẩm duy nhất, ankan sẽ là ankan đối xứng.
2. Dẫn xuất đi, tri...halogen:
- Ankan + Halogen tỉ lệ 1 : 2, 1 : 3, ...
- Yêu cầu của đề: xác định công thức của dẫn xuất halogen.
- Dữ kiện: đề bài sẽ cho %C, %H, hay %Halogen và CTPT của ankan.
- PT:
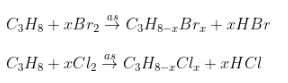
- Công thức tính: (ví dụ với ankan là C3H8)
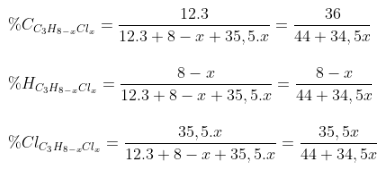
Xác định x.
IV. Các công thức hoá học lớp 11: Phản ứng cracking
- Phương trình:
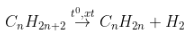
Ankan Anken
hoặc 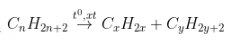 (x + y = n)
(x + y = n)
Anken Ankan khác
Ví dụ:
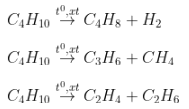
- Từ ankan đầu, sau phản ứng có thể thu nhiều chất sản phẩm.
- Khối lượng hỗn hợp trước và sau phản ứng không đổi:
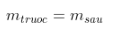
=> 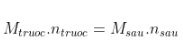 hay
hay 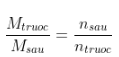
- Bảo toàn nguyên tố C và H: Khi đề bài cho đốt cháy hỗn hợp sau phản ứng ta qui về đốt cháy hỗn hợp trước phản ứng (một chất sẽ đơn giản hơn nhiều chất).
- Số mol hỗn hợp: 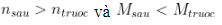
Ví dụ: 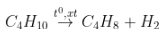
1 1 1
=> 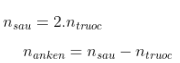
- Hiệu suất phản ứng: 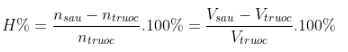
(Các công thức liên quan đến số mol ta có thể thay thế bằng thể tích).
V. Các công thức hoá học lớp 11: Phản ứng cộng
- Phản ứng cộng phá vỡ liên kết π. Liên kết π là liên kết kết kém bền, nên chúng dễ bị đứt ra để tạo thành liên kết các nguyên tử khác.
1. Cộng H2:
- Chất xúc tác như: Ni, Pt, Pd, ở nhiệt độ thích hợp.
- Sơ đồ:
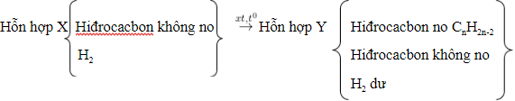
- PTTQ: 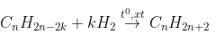
Với k là số liên kết π trong phân tử, 1π sẽ cộng với 1H2.
- Tùy vào hiệu suất và tỉ lệ của phản ứng mà hỗn hợp Y có thể còn hiđrocacbon không no dư hoặc hiđro dư hoặc cả hai còn dư.
- Trong phản ứng cộng H2, số mol khí sau phản ứng luôn giảm (nY < nX) và bằng mol H2 phản ứng: 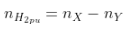
- Bảo toàn khối lượng: 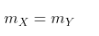
- 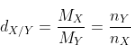 (luôn lớn hơn 1).
(luôn lớn hơn 1).
- Hỗn hợp X và Y chỉ thay đổi về chất nhưng vẫn bảo toàn H và C, nên thay vì đốt cháy Y ta có thể đốt cháy X. Sử dụng định luật bảo toàn nguyên tố như bài toán đốt cháy.
- 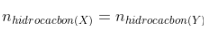
a) Xét hiđrocacbon X là anken:
- Sơ đồ:
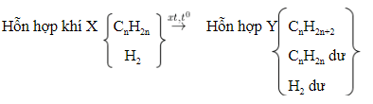
- Phương trình:
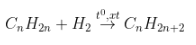
- 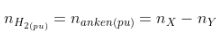 (= số mol khí giảm).
(= số mol khí giảm).
b) Xét hiđrocacbon X là anken:
- Sơ đồ:
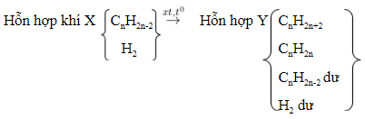
- Phương trình tổng quát:
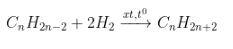
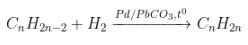
- 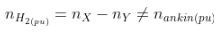
2. Cộng brom:
- Phương trình:
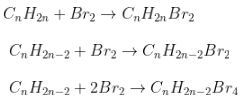
- Công thức:
+ m bình tăng = m hiđrocacbon không no
+ Vkhí thoát ra = V hiđrocacbon no
+ nπ = 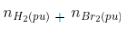
VI. Các công thức hoá học lớp 11: Bài tập về phản ứng của ankin có liên kết ba đầu mạch với dung dịch AgNO3/NH3
- Phản ứng xảy ra chỉ với ankin có nối ba đầu mạch (ank – 1 – in).
- PTTQ:
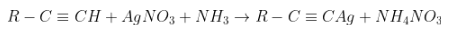
Kết tủa vàng
Phản ứng với tỉ lệ 1:1
- Riêng với axetilen:
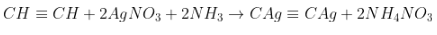
Phản ứng với tỉ lệ 1:2.
- Gọi 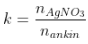 ,
,
+ k = 1: hỗn hợp chỉ gồm ank – 1 – in,
+ 1 < k < 2, hỗn hợp gồm C2H2 (hoặc ankin có 2 nối ba đầu mạch) và ank – 1 – in.
- Mkết tủa = Mankin + 107x (với x là số nối ba đầu mạch).
Các công thức hoá học lớp 11
Nếu nắm vững được các phản ứng và Các công thức hoá học lớp 11 trên đây, các em sẽ giải được các dạng bài tập về hiđrocacbon. Hãy luyện tập và vận dụng thật nhiều các em nhé!